글리세롤 3-인산 탈수소효소
글리세롤 3-인산 탈수소효소(영어: glycerol 3-phosphate dehydrogenase, GPDH)는 다이하이드록시아세톤 인산을 sn-글리세롤 3-인산으로 가역적 산화환원 전환하는 반응을 촉매하는 효소이다.[2]
| 글리세롤 3-인산 탈수소효소 (NAD+) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 사람의 글리세롤 3-인산 탈수소효소의 결정학적 구조[1] | |||||||||
| 식별자 | |||||||||
| EC 번호 | 1.1.1.8 | ||||||||
| CAS 번호 | 9075-65-4 | ||||||||
| 데이터베이스 | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB 구조 | RCSB PDB PDBj PDBe PDBsum | ||||||||
| 유전자 온톨로지 | AmiGO / QuickGO | ||||||||
| |||||||||
| NAD-의존성 글리세롤 3-인산 탈수소효소 N-말단 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
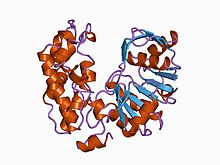 아르트로박터 종의 n-(1-D-카복실레틸)-L-노르발린 탈수소효소의 결정 구조 | |||||||||
| 식별자 | |||||||||
| 상징 | NAD_Gly3P_dh_N | ||||||||
| Pfam | PF01210 | ||||||||
| Pfam clan | CL0063 | ||||||||
| InterPro | IPR011128 | ||||||||
| PROSITE | PDOC00740 | ||||||||
| SCOP | 1m66 | ||||||||
| SUPERFAMILY | 1m66 | ||||||||
| |||||||||
| NAD-의존성 글리세롤 3-인산 탈수소효소 C-말단 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
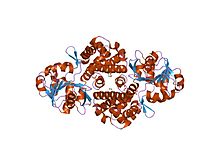 아르카에오글로부스 풀기두스(archaeoglobus fulgidus)의 글리세롤 3-=인산 탈수소효소의 구조 | |||||||||
| 식별자 | |||||||||
| 상징 | NAD_Gly3P_dh_C | ||||||||
| Pfam | PF07479 | ||||||||
| Pfam clan | CL0106 | ||||||||
| InterPro | IPR006109 | ||||||||
| PROSITE | PDOC00740 | ||||||||
| SCOP | 1m66 | ||||||||
| SUPERFAMILY | 1m66 | ||||||||
| |||||||||
글리세롤 3-인산 탈수소효소는 탄수화물 대사와 지질 대사의 사이에서 중요한 연결 고리 역할을 한다. 또한 미토콘드리아의 전자전달계로의 주요 전자 공급원이다.
글리세롤 3-인산 탈수소효소에 대한 이전 용어로는 알파 글리세롤 3-인산 탈수소효소 및 글리세롤인산 탈수소효소 등이 있다. 그러나 글리세롤 3-인산 탈수소효소는 기질이 알코올이 아닌 알데하이드인 글리세르알데하이드 3-인산 탈수소효소(GAPDH)와 동일하지 않다.
대사 기능
편집글리세롤 3-인산 탈수소효소는 지질 생합성에서 중요한 역할을 한다. 다이하이드록시아세톤 인산을 글리세롤 3-인산으로 환원함으로써 글리세롤 3-인산 탈수소효소는 글리세롤 3-인산을 글리세롤로 신속하게 탈인산화한다.[3] 또한 글리세롤 3-인산 탈수소효소는 미토콘드리아 내막을 가로질러 산화환원 전위를 유지하는 데 관여하는 효소 중 하나이다.[3]
반응
편집NAD+/NADH 조효소 커플은 물질대사의 산화환원반응을 위한 전자 저장소 역할을 하며 한 반응에서 다른 반응으로 전자를 운반한다.[5] 이러한 물질대사 반응의 대부분은 미토콘드리아에서 일어난다. 추가적인 사용을 위해 NAD+를 재생하려면 세포질의 NADH 풀을 재산화해야 한다. 미토콘드리아 내막은 NADH와 NAD+ 모두에 대해 불투과성이므로 이들은 세포질과 미토콘드리아 기질 사이에서 자유롭게 교환될 수 없다.[4]
막을 가로질러 이 환원 당량을 이동시키는 한 가지 방법은 2가지 형태의 글리세롤 3-인산 탈수소효소를 사용하는 글리세롤 3-인산 셔틀을 이용하는 것이다.
- 세포질의 글리세롤 3-인산 탈수소효소(GPDH) 또는 GPD1은 세포질과 마주하는 미토콘드리아 외막에 국한되어 있으며 다이하이드록시아세톤 인산을 글리세롤 3-인산으로 환원하는 것을 촉매한다.
- 이와 함께 미토콘드리아의 글리세롤 3-인산 탈수소효소(GPDH) 또는 GPD2는 세포질을 내려다보는 미토콘드리아 내막의 바깥쪽 표면에 묻혀 있으며 글리세롤 3-인산을 다이하이드록시아세톤 인산으로 산화하는 것을 촉매한다.[6]
세포질의 글리세롤 3-인산 탈수소효소(가용성) 및 미토콘드리아의 글리세롤 3-인산 탈수소효소에 의해 촉매되는 반응은 다음과 같다.
변형
편집글리세롤 3-인산 탈수소효소는 다음과 같이 두 가지 형태가 있다.
| 효소 | 단백질 | 유전자 | |||||
|---|---|---|---|---|---|---|---|
| EC 번호 | 이름 | 공여체 / 수용체 | 이름 | 세포 내 위치 | 약어 | 이름 | 기호 |
| 1.1.1.8 | 글리세롤 3-인산 탈수소효소 | NADH / NAD+ | 글리세롤 3-인산 탈수소효소 [NAD+] | 세포질 | GPDH-C | 글리세롤 3-인산 탈수소효소 1 (가용성) | GPD1 |
| 1.1.5.3 | 글리세롤 3-인산 탈수소효소 | 퀴놀 / 퀴논 | 글리세롤 3-인산 탈수소효소 | 미토콘드리아 | GPDH-M | 글리세롤 3-인산 탈수소효소 2 (미토콘드리아) | GPD2 |
다음의 사람 유전자는 글리세롤 3-인산 탈수소효소 활성을 갖는 단백질을 암호화한다.
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
GPD1
편집세포질의 글리세롤 3-인산 탈수소효소(GPD1)는 다이하이드록시아세톤 인산을 글리세롤 3-인산으로 환원시키는 NAD+ 의존성 효소이다.[8] 동시에 NADH는 다음의 반응에서 NAD+로 산화된다.
결과적으로 NAD+는 추가적인 대사를 위해 재생된다.
GPD1은 2개의 소단위체로 구성되어 있으며,[9] 다음과 같은 상호작용을 통해 다이하이드록시아세톤 인산 및 NAD+와 반응한다.
GPD2
편집미토콘드리아의 글리세롤 3-인산 탈수소효소(GPD2)는 글리세롤 3-인산에서 다이하이드록시아세톤 인산으로의 비가역적 산화를 촉매하고 동시에 2개의 전자를 FAD로 전달하여 FADH2를 생성한다. GPD2는 4개의 동일한 소단위체들로 구성된다.[10]
환경 스트레스에 대한 반응
편집글리세롤 3-인산 셔틀
편집미토콘드리아의 글리세롤 3-인산 탈수소효소와 세포질의 글리세롤 3-인산 탈수소효소는 서로 협력하여 작동한다. 세포질의 글리세롤 3-인산 탈수소효소에 의해 NADH는 NAD+로 산화되고 다이하이드록시아세톤 인산이 글리세롤 3-인산으로 전환된다. 일단 글리세롤 3-인산이 미토콘드리아 내막을 통해 이동하면 퀴논을 산화제로 사용하고 FAD를 보조 인자로 사용하는 미토콘드리아의 글리세롤 3-인산 탈수소효소에 의해 다이하이드록시아세톤 인산으로 산화될 수 있다. 결과적으로 ATP 1분자에 필적하는 에너지의 순손실이 일어난다.[7]
질병에서의 역할
편집NAD+/NADH 퍼텐셜을 유지하는 글리세롤 3-인산 탈수소효소의 기본적인 역할과 지질 대사에서의 역할을 글리세롤 3-인산 탈수소효소를 비만과 같은 지질 불균형 질환의 요인으로 만든다.
- 글리세롤 3-인산 탈수소효소의 활성 향상, 특히 GPD2는 글리세롤의 생산을 증가시킨다. 글리세롤은 지질 대사의 주요 소단위체이기 때문에 글리세롤이 풍부하면 세포 수준에서 트라이글리세라이드의 축적이 쉽게 증가할 수 있다. 그 결과 지방 조직이 형성되어 비만에 유리한 지방이 축적되는 경향이 있다.[12]
- 글리세롤 3-인산 탈수소효소는 또한 브루가다 증후군에서 역할을 하는 것으로 밝혀졌다. GPD1을 암호화하는 유전자의 돌연변이는 전자전달계에 결함을 일으키는 것으로 입증되었다. 세포에서 NAD+/NADH 수준과의 이러한 충돌은 심장 나트륨 이온 통로 조절의 결함에 기여하는 것으로 믿어지며 유아기에 치명적인 부정맥을 유발할 수 있다.[13]
약리학적 표적
편집미토콘드리아의 글리세롤 3-인산 탈수소효소는 제2형 당뇨병의 1차 약물인 메트포르민에 의해 저해되는 것으로 생각된다.[14]
생물학적 연구
편집사르코파가 바르바타(Sarcophaga barbata)는 미토콘드리아에서 글리세롤 3-인산의 산화를 연구하는 데 사용되었다. 글리세롤 3-인산은 피루브산과는 달리 미토콘드리아 기질로 들어가지 않는 것으로 밝혀졌다. 이것은 미토콘드리아 내막에 있는 글리세롤 3-인산 플라보단백질 산화환원효소를 찾는 데 도움을 준다.
구조
편집글리세롤 3-인산 탈수소효소는 두 개의 단백질 도메인으로 구성된다. N-말단 도메인은 NAD 결합 도메인이고, C-말단 도메인은 기질 결합 도메인으로 작용한다.[15] 그러나 글리세롤 3-인산 탈수소효소는 RNA 결합 및 안정성의 조절을 포함하여 여러 달빛(moonlighting) 활성을 나타낼 수 있기 때문에 이량체 및 사량체 계면 잔기는 글리세롤 3-인산 탈수소효소와 RNA의 결합에 관여한다.[16]
같이 보기
편집각주
편집- ↑ PDB 1X0V; Ou X, Ji C, Han X, Zhao X, Li X, Mao Y, Wong LL, Bartlam M, Rao Z (Mar 2006). “Crystal structures of human glycerol 3-phosphate dehydrogenase 1 (GPD1)”. 《Journal of Molecular Biology》 357 (3): 858–69. doi:10.1016/j.jmb.2005.12.074. PMID 16460752.
- ↑ Ou X, Ji C, Han X, Zhao X, Li X, Mao Y, Wong LL, Bartlam M, Rao Z (Mar 2006). “Crystal structures of human glycerol 3-phosphate dehydrogenase 1 (GPD1)”. 《Journal of Molecular Biology》 357 (3): 858–69. doi:10.1016/j.jmb.2005.12.074. PMID 16460752.
- ↑ 가 나 Harding JW, Pyeritz EA, Copeland ES, White HB (Jan 1975). “Role of glycerol 3-phosphate dehydrogenase in glyceride metabolism. Effect of diet on enzyme activities in chicken liver”. 《The Biochemical Journal》 146 (1): 223–9. doi:10.1042/bj1460223. PMC 1165291. PMID 167714.
- ↑ 가 나 Geertman JM, van Maris AJ, van Dijken JP, Pronk JT (Nov 2006). “Physiological and genetic engineering of cytosolic redox metabolism in Saccharomyces cerevisiae for improved glycerol production”. 《Metabolic Engineering》 8 (6): 532–42. doi:10.1016/j.ymben.2006.06.004. PMID 16891140.
- ↑ Ansell R, Granath K, Hohmann S, Thevelein JM, Adler L (May 1997). “The two isoenzymes for yeast NAD+-dependent glycerol 3-phosphate dehydrogenase encoded by GPD1 and GPD2 have distinct roles in osmoadaptation and redox regulation”. 《The EMBO Journal》 16 (9): 2179–87. doi:10.1093/emboj/16.9.2179. PMC 1169820. PMID 9171333.
- ↑ Kota V, Rai P, Weitzel JM, Middendorff R, Bhande SS, Shivaji S (Sep 2010). “Role of glycerol-3-phosphate dehydrogenase 2 in mouse sperm capacitation”. 《Molecular Reproduction and Development》 77 (9): 773–83. doi:10.1002/mrd.21218. PMID 20602492. S2CID 19691537.
- ↑ 가 나 Stryer, Lubert; Berg, Jeremy Mark; Tymoczko, John L. (2002). 〈Chapter 18.5: Glycerol 3-Phosphate Shuttle〉. 《Biochemistry》. San Francisco: W.H. Freeman. ISBN 0-7167-4684-0.
- ↑ Guindalini C, Lee KS, Andersen ML, Santos-Silva R, Bittencourt LR, Tufik S (Jan 2010). “The influence of obstructive sleep apnea on the expression of glycerol-3-phosphate dehydrogenase 1 gene”. 《Experimental Biology and Medicine》 235 (1): 52–6. doi:10.1258/ebm.2009.009150. PMID 20404019. S2CID 207194967. 2011년 7월 24일에 원본 문서에서 보존된 문서. 2011년 5월 16일에 확인함.
- ↑ Bunoust O, Devin A, Avéret N, Camougrand N, Rigoulet M (Feb 2005). “Competition of electrons to enter the respiratory chain: a new regulatory mechanism of oxidative metabolism in Saccharomyces cerevisiae”. 《The Journal of Biological Chemistry》 280 (5): 3407–13. doi:10.1074/jbc.M407746200. PMID 15557339.
- ↑ Kota V, Dhople VM, Shivaji S (Apr 2009). “Tyrosine phosphoproteome of hamster spermatozoa: role of glycerol-3-phosphate dehydrogenase 2 in sperm capacitation”. 《Proteomics》 9 (7): 1809–26. doi:10.1002/pmic.200800519. PMID 19333995. S2CID 9248320.
- ↑ Kumar S, Kalyanasundaram GT, Gummadi SN (Feb 2011). “Differential response of the catalase, superoxide dismutase and glycerol-3-phosphate dehydrogenase to different environmental stresses in Debaryomyces nepalensis NCYC 3413”. 《Current Microbiology》 62 (2): 382–7. doi:10.1007/s00284-010-9717-z. PMID 20644932. S2CID 41613712.
- ↑ Xu SP, Mao XY, Ren FZ, Che HL (Feb 2011). “Attenuating effect of casein glycomacropeptide on proliferation, differentiation, and lipid accumulation of in vitro Sprague-Dawley rat preadipocytes”. 《Journal of Dairy Science》 94 (2): 676–83. doi:10.3168/jds.2010-3827. PMID 21257036.
- ↑ Van Norstrand DW, Valdivia CR, Tester DJ, Ueda K, London B, Makielski JC, Ackerman MJ (Nov 2007). “Molecular and functional characterization of novel glycerol-3-phosphate dehydrogenase 1 like gene (GPD1-L) mutations in sudden infant death syndrome”. 《Circulation》 116 (20): 2253–9. doi:10.1161/CIRCULATIONAHA.107.704627. PMC 3332545. PMID 17967976.
- ↑ Ferrannini E (Oct 2014). “The target of metformin in type 2 diabetes”. 《The New England Journal of Medicine》 371 (16): 1547–8. doi:10.1056/NEJMcibr1409796. PMID 25317875.
- ↑ Suresh S, Turley S, Opperdoes FR, Michels PA, Hol WG (May 2000). “A potential target enzyme for trypanocidal drugs revealed by the crystal structure of NAD-dependent glycerol-3-phosphate dehydrogenase from Leishmania mexicana”. 《Structure》 8 (5): 541–52. doi:10.1016/s0969-2126(00)00135-0. PMID 10801498.
- ↑ White MR, Khan MM, Deredge D, Ross CR, Quintyn R, Zucconi BE, Wysocki VH, Wintrode PL, Wilson GM, Garcin ED (Jan 2015). “A dimer interface mutation in glyceraldehyde-3-phosphate dehydrogenase regulates its binding to AU-rich RNA”. 《The Journal of Biological Chemistry》 (영어) 290 (3): 1770–85. doi:10.1074/jbc.M114.618165. PMC 4340419. PMID 25451934.
더 읽을거리
편집- Baranowski T (1963). 〈α-Glycerophosphate dehydrogenase〉. Boyer PD, Lardy H, Myrbäck K. 《The Enzymes》 2판. New York: Academic Press. 85–96쪽.
- Brosemer RW, Kuhn RW (May 1969). “Comparative structural properties of honeybee and rabbit alpha-glycerophosphate dehydrogenases”. 《Biochemistry》 8 (5): 2095–105. doi:10.1021/bi00833a047. PMID 4307630.
- O'Brien SJ, MacIntyre RJ (Oct 1972). “The -glycerophosphate cycle in Drosophila melanogaster. I. Biochemical and developmental aspects”. 《Biochemical Genetics》 7 (2): 141–61. doi:10.1007/BF00486085. PMID 4340553. S2CID 22009695.
- Warkentin DL, Fondy TP (Jul 1973). “Isolation and characterization of cytoplasmic L-glycerol-3-phosphate dehydrogenase from rabbit-renal-adipose tissue and its comparison with the skeletal-muscle enzyme”. 《European Journal of Biochemistry》 36 (1): 97–109. doi:10.1111/j.1432-1033.1973.tb02889.x. PMID 4200180.
- Albertyn J, van Tonder A, Prior BA (Aug 1992). “Purification and characterization of glycerol-3-phosphate dehydrogenase of Saccharomyces cerevisiae”. 《FEBS Letters》 308 (2): 130–2. doi:10.1016/0014-5793(92)81259-O. PMID 1499720. S2CID 39643279.
- Koekemoer TC, Litthauer D, Oelofsen W (Jun 1995). “Isolation and characterization of adipose tissue glycerol-3-phosphate dehydrogenase”. 《The International Journal of Biochemistry & Cell Biology》 27 (6): 625–32. doi:10.1016/1357-2725(95)00012-E. PMID 7671141.
- Påhlman IL, Larsson C, Averét N, Bunoust O, Boubekeur S, Gustafsson L, Rigoulet M (Aug 2002). “Kinetic regulation of the mitochondrial glycerol-3-phosphate dehydrogenase by the external NADH dehydrogenase in Saccharomyces cerevisiae”. 《The Journal of Biological Chemistry》 277 (31): 27991–5. doi:10.1074/jbc.M204079200. PMID 12032156.
- Overkamp KM, Bakker BM, Kötter P, van Tuijl A, de Vries S, van Dijken JP, Pronk JT (May 2000). “In vivo analysis of the mechanisms for oxidation of cytosolic NADH by Saccharomyces cerevisiae mitochondria”. 《Journal of Bacteriology》 182 (10): 2823–30. CiteSeerX 10.1.1.335.5313. doi:10.1128/JB.182.10.2823-2830.2000. PMC 101991. PMID 10781551.
- Dawson AG, Cooney GJ (Jul 1978). “Reconstruction of the alpha-glycerolphosphate shuttle using rat kidney mitochondria”. 《FEBS Letters》 91 (2): 169–72. doi:10.1016/0014-5793(78)81164-8. PMID 210038.
- Opperdoes FR, Borst P, Bakker S, Leene W (Jun 1977). “Localization of glycerol-3-phosphate oxidase in the mitochondrion and particulate NAD+-linked glycerol-3-phosphate dehydrogenase in the microbodies of the bloodstream form to Trypanosoma brucei”. 《European Journal of Biochemistry》 76 (1): 29–39. doi:10.1111/j.1432-1033.1977.tb11567.x. PMID 142010.
- Eswaramoorthy S, Bonanno JB, Burley SK, Swaminathan S (Jun 2006). “Mechanism of action of a flavin-containing monooxygenase”. 《Proceedings of the National Academy of Sciences of the United States of America》 103 (26): 9832–7. Bibcode:2006PNAS..103.9832E. doi:10.1073/pnas.0602398103. PMC 1502539. PMID 16777962.
외부 링크
편집이 문서는 현재 퍼블릭 도메인에 속하는 Pfam 및 InterPro: IPR011128의 내용을 기초로 작성된 글이 포함되어 있습니다.
이 문서는 현재 퍼블릭 도메인에 속하는 Pfam 및 InterPro: IPR006109의 내용을 기초로 작성된 글이 포함되어 있습니다.