아세틸-CoA
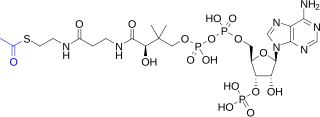
아세틸-CoA(영어: acetyl-CoA) 또는 아세틸 조효소 A(영어: acetyl coenzyme A)는 단백질, 탄수화물 및 지질 대사 등 많은 생화학 반응에 참여하는 분자이다.[1] 아세틸-CoA의 주요 기능은 아세틸기를 시트르산 회로에 전달하여 에너지 생산을 위해 산화되도록 하는 것이다. 조효소 A(CoA-SH 또는 CoA)에서 판토텐산의 하이드록시기는 3′-포스포아데노신 이인산과 인산에스터(인산에스테르) 결합을 하고 있으며, 판토텐산의 카복실기는 β-메르캅토에틸아민과 아마이드 결합을 하고 있다.[2] 아세틸-CoA의 아세틸기(오른쪽 구조식에서 파란색으로 표시)는 β-메르캅토에틸아민 부분의 -SH기와 싸이오에스터(싸이오에스테르) 결합을 형성한다. 이러한 싸이오에스터 결합은 특히 반응성이 강한 "고에너지" 결합이다. 싸이오에스터 결합의 가수분해는 발열 반응(−31.5 kJ/mol)이다.
| |
| |
| 이름 | |
|---|---|
| IUPAC 이름
S-[2-[3-[[(2R)-4-[[[(2R,3S,4R,5R)-5-(6-aminopurin-9-yl)-4-hydroxy-3-phosphonooxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl]oxy-2-hydroxy-3,3-dimethylbutanoyl]amino]propanoylamino]ethyl] ethanethioate
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.000.719 |
| KEGG | |
| MeSH | Acetyl+Coenzyme+A |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C23H38N7O17P3S | |
| 몰 질량 | 809.57 g·mol−1 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
CoA는 해당과정을 통한 탄수화물의 분해와 β 산화를 통한 지방산의 분해에 의해 아세틸-CoA로 아세틸화된다. 아세틸-CoA는 시트르산 회로로 들어가서, 아세틸기가 이산화 탄소(CO2)와 물(H2O)로 산화되고, 방출되는 에너지를 이용해서 아세틸기 1분자당 11분자의 ATP와 1분자의 GTP를 생성한다.
콘라드 블로흐와 페오드르 리넨은 아세틸-CoA와 지방산 대사의 관련성을 발견한 공로로 1964년에 노벨 생리학·의학상을 수상했고 프리츠 리프먼은 보조 인자인 조효소 A를 발견한 공로로 1953년에 노벨 생리학·의학상을 수상했다.
직접적인 합성
편집CoA의 아세틸화는 탄소 공급원에 의해 결정된다.[3][4]
미토콘드리아 밖에서
편집- 포도당의 농도가 높을 때 해당과정이 빠르게 일어나서 시트르산 회로에서 생성되는 시트르산의 양이 증가한다. 세포질에서 시트르산은 ATP 시트르산 분해효소(ATP citrate lyase)에 의해 아세틸-CoA와 옥살아세트산으로 분해되고, 이 과정에서 ATP는 ADP와 Pi로 가수분해된다.[5][6]
- 포도당의 농도가 낮을 때:
- CoA는 아세틸-CoA 합성효소에 의해 아세트산을 사용하여 아세틸화되고, ATP 가수분해와 짝지워진다.[7]
- 또한 에탄올은 알코올 탈수소효소에 의해 CoA의 아세틸화를 위한 탄소 공급원 역할을 한다.[8]
- 발린, 류신, 아이소류신과 같은 가지사슬 케톤 생성 아미노산의 분해가 일어난다. 이들 아미노산들은 가지사슬 아미노기 전이효소(branched-chain aminotransferase)에 의해 α-케토산으로 전환되고, 결국 가지사슬 α-케토산 탈수소효소 복합체(branched-chain α-ketoacid dehydrogenase complex)에 의해 산화적 탈카복실화를 통해 아이소발레릴-CoA로 전환된다. 아이소발레릴-CoA는 아세틸-CoA 및 아세토아세트산으로 분해되기 전에 다른 CoA 유도체를 형성하기 위해 탈수소화, 카복실화 및 수화를 거친다.[9]
미토콘드리아 내에서
편집- 포도당의 농도가 높을 때, 해당과정을 통해 아세틸-CoA가 생성된다.[10] 피루브산은 산화적 탈카복실화를 거치면서 카복실기(이산화 탄소)를 소실하고 아세틸-CoA를 형성하는데, 이 과정에서 33.5 kJ/mol의 에너지를 방출한다. 피루브산이 아세틸-CoA로 산화적 탈카복실화되는 반응은 피루브산 탈수소효소 복합체에 의해 촉매된다. NADH의 산화로 방출된 고에너지 전자는 미토콘드리아 내막에 있는 일련의 전자 운반체의 산화, 환원에 의해 차례로 전달되며 최종 전자수용체인 산소(O2)가 전자를 받아 물(H2O)로 환원된다.[11] 피루브산과 아세틸-CoA 사이의 다른 전환이 가능하다. 예를 들어, 피루브산 포름산 분해효소(pyruvate formate lyase)는 피루브산을 아세틸-CoA와 포름산으로 불균등화시킨다.
- 포도당의 농도가 낮을 때, 아세틸-CoA의 생성은 지방산의 β 산화와 관련이 있다. 먼저 지방산은 아실-CoA로 전환된다. 아실-CoA는 4가지 효소, 즉 아실-CoA 탈수소효소, 에노일-CoA 수화효소, β-하이드록시아실-CoA 탈수소효소, 아실-CoA 아세틸기 전이효소(싸이올레이스)에 의해 촉매되는 4단계의 탈수소화, 수화, 산화, 싸이올 분해 과정에서 분해된다. 이 과정에서 아세틸-CoA와 탄소 원자가 2개가 적은 새로운 아실-CoA가 생성된다.[12]
기능
편집다양한 대사 경로의 중간생성물
편집- 식물과 동물에서, 세포질의 아세틸-CoA는 ATP 시트르산 분해효소(ATP citrate lyase)에 의해 합성된다.[13] 동물의 경우 혈당량이 높으면 포도당은 세포질에서 피루브산으로 분해되고(해당과정), 미토콘드리아에서 아세틸-CoA로 전환된다. 아세틸-CoA가 과다하면 시트르산의 양이 증가하고, 여분의 시트르산은 세포질로 운반되어 세포질의 아세틸-CoA의 양을 증가시킨다.
- 시트르산 회로:
- 지방산 대사:
- 아세틸-CoA는 탄수화물의 분해(해당과정 및 피루브산의 산화)와 지방의 분해(β 산화)에 의해 생성된다. 아세틸-CoA는 미토콘드리아 기질에서 옥살아세트산과 결합해서 시트르산을 형성하여 시트르산 회로를 시작한다.[14][15]
- 아세틸-CoA 2분자가 축합하여 아세토아세틸-CoA를 형성하여 후속 반응들을 통하여 아세토아세트산과 β-하이드록시뷰티르산을 생성한다.[14] 아세토아세트산, β-하이드록시뷰티르산 및 이들의 자발적인 분해 산물인 아세톤[16]은 케톤체로 알려져 있다. 케톤체는 간에 의해서 혈액으로 방출된다. 미토콘드리아가 있는 모든 세포는 혈액으로부터 흡수한 케톤체를 아세틸-CoA로 다시 전환할 수 있으며, 이렇게 형성된 아세틸-CoA를 시트르산 회로에서 연료로 사용할 수 있다. 포유동물은 아세틸-CoA를 포도당신생합성의 전구물질로 사용할 수 없다. 유리 지방산과는 달리 케톤체는 혈액뇌장벽을 통과할 수 있어서 보통 포도당을 연료로 사용하는 뇌와 같은 중추신경계 세포에서 연료로 사용될 수 있다.[14] 기아, 저탄수화물 식이, 장기간의 심한 운동, 치료 받지 않은 제1형 당뇨병에서 혈액 중에 케톤체의 농도가 높아지는 상태를 케톤증(ketosis)이라 하고, 통제되지 않은 제1형 당뇨병의 극단적인 형태는 케톤산증(ketoacidosis)이라 한다.
- 반면에 혈액 내 인슐린의 농도가 높고 글루카곤의 농도가 낮을 때(즉, 식사 후), 해당과정에 의해 생성된 아세틸-CoA는 미토콘드리아 기질에서 옥살아세트산과 축합하여 시트르산을 생성한다. 그러나 시트르산 회로를 통해 이산화 탄소(O2)와 물(H2O)로 전환되는 대신에, 시트르산은 미토콘드리아 기질에서 세포질로 운반된다.[14] 세포질에서 시트르산은 ATP 시트르산 분해효소에 의해 아세틸-CoA와 옥살아세트산으로 분해된다. 옥살아세트산은 말산으로 전환되어 미토콘드리아 기질로 다시 돌아오고, 더 많은 아세틸-CoA의 아세틸기를 미토콘드리아 밖으로 운반하기 위해 말산은 옥살아세트산으로 전환된다.[17] 세포질의 아세틸-CoA는 지방산 합성의 첫 단계인 아세틸-CoA 카복실화효소에 의한 말로닐-CoA로의 카복실화를 통해 지방산을 합성하는데 사용될 수 있다.[17][18] 이러한 전환은 간, 지방 조직, 젖을 분비하는 젖샘에서 주로 일어난다. 지방산은 글리세롤과 결합하여 대부분의 동물에서 연료의 주된 저장 형태인 트라이글리세라이드를 형성한다. 또한 지방산은 모든 세포막의 지질 이중층을 구성하는 인지질의 구성 요소이다.[14]
- 식물에서 새로이 생성되는 지방산의 합성은 색소체에서 일어난다. 종자의 발아 및 어린 식물의 초기 생장을 지원하기 위해 많은 종자들은 기름(oil)을 저장하고 있다.
- 세포질의 아세틸-CoA는 아세토아세틸-CoA와 축합하여 β-하이드록시-β-메틸글루타릴-CoA(HMG-CoA)를 형성한다. 이 반응은 콜레스테롤 합성을 조절하는 속도제한단계이다.[14] 콜레스테롤은 동물 세포막의 구성 성분으로 그대로 사용되거나, 스테로이드 호르몬, 담즙산, 비타민 D를 합성하는데 사용될 수 있다.[14][18]
- 아세틸-CoA는 세포질에서 아세틸-CoA 카복실화효소에 의해 카복실화되어 말로닐-CoA가 된다. 말로닐-CoA는 플라보노이드 및 그와 관련된 폴리케타이드(polyketide)를 합성하고, 단백질과 기타 식물화학물질(phytochemical)을 말로닐화 하는데 쓰인다. 말로닐-CoA는 왁스, 큐티클을 생성하기 위한 지방산의 신장과 배추속 식물의 종자 기름 생성에 필요한 기질인 말로닐-CoA를 생성한다.[19] 세스퀴테르펜(sesquiterpene), 브라시노스테로이드(식물 호르몬) 및 막 스테롤이 역시 이러한 방법으로 합성된다.
- 스테로이드 합성:
- 아세틸-CoA는 β-하이드록시-β-메틸글루타릴-CoA의 합성에 관여함으로써 메발론산 경로에 참여한다. 메발론산 경로(mevalonate pathway)는 2분자의 아세틸-CoA가 축합반응을 통해 이소프레노이드를 합성하는 경로이다. 이 경로의 속도제한단계 효소는 HMG-CoA 환원효소(HMG-CoA reductase)이다. 동물의 경우 HMG-CoA는 콜레스테롤과 케톤체 합성의 주요 전구체이다.
- 아세틸콜린 합성:
- 아세틸-CoA는 또한 신경전달물질인 아세틸콜린의 생합성에 주요 성분이다. 콜린 아세틸기 전이효소에 의해 콜린은 아세틸-CoA와 반응하여 아세틸콜린과 조효소 A(CoA)를 생성한다.
- 멜라토닌 합성
- 아세틸화
- 다른 자리 입체성 조절인자
- 아세틸-CoA는 피루브산 탈수소효소 키네이스의 다른 자리 입체성 조절인자로 작용한다. 이는 아세틸-CoA 대 CoA의 비율을 통해 조절된다. 아세틸-CoA의 농도 증가는 피루브산 탈수소효소 키네이스를 활성화시킨다.[21]
- 아세틸-CoA는 또한 피루브산 카복실화효소의 다른 자리 입체성 활성인자이다.[22]
같이 보기
편집각주
편집- ↑ “Acetyl CoA Crossroads”. 《chemistry.elmhurst.edu》. 2016년 11월 15일에 원본 문서에서 보존된 문서. 2016년 11월 8일에 확인함.
- ↑ “Fatty Acids -- Structure of Acetyl CoA”. 《library.med.utah.edu》. 2017년 5월 31일에 원본 문서에서 보존된 문서. 2017년 6월 2일에 확인함.
- ↑ Hynes, Michael J.; Murray, Sandra L. (2010년 7월 1일). “ATP-Citrate Lyase Is Required for Production of Cytosolic Acetyl Coenzyme A and Development in Aspergillus nidulans”. 《Eukaryotic Cell》 (영어) 9 (7): 1039–1048. doi:10.1128/EC.00080-10. ISSN 1535-9778. PMC 2901662. PMID 20495057. 2018년 6월 2일에 원본 문서에서 보존된 문서. 2018년 8월 1일에 확인함.
- ↑ Wellen, Kathryn E.; Thompson, Craig B. (2012년 4월 1일). “A two-way street: reciprocal regulation of metabolism and signalling”. 《Nature Reviews Molecular Cell Biology》 (영어) 13 (4): 270–276. doi:10.1038/nrm3305. ISSN 1471-0072. PMID 22395772.
- ↑ Storey, Kenneth B. (2005년 2월 25일). 《Functional Metabolism: Regulation and Adaptation》 (영어). John Wiley & Sons. ISBN 9780471675570.
- ↑ “ACLY ATP citrate lyase [Homo sapiens (human)] - Gene - NCBI”. 《www.ncbi.nlm.nih.gov》. 2016년 11월 6일에 확인함.
- ↑ Ragsdale, S. W. (2004). “Life with carbon monoxide”. 《CRC Critical Reviews in Biochemistry and Molecular Biology》 39: 165–195.
- ↑ Chatterjea (2004년 1월 1일). 《Textbook of Biochemistry for Dental/Nursing/Pharmacy Students》 (영어). Jaypee Brothers Publishers. ISBN 9788180612046.[깨진 링크(과거 내용 찾기)]
- ↑ 가 나 Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). 《Biochemistry》 5판. W. H. Freeman. ISBN 0716730510.
- ↑ Blackstock, James C. (2014년 6월 28일). 《Guide to Biochemistry》 (영어). Butterworth-Heinemann. ISBN 9781483183671.
- ↑ Nelson D.L., Cox M.M. (2005). “16 The Citric Acid Cycle”. Lehninger Principles of Biochemistry (영어) 4판. W.H. Freeman and Company. ISBN 0-7167-4339-6.
- ↑ Houten, Sander Michel; Wanders, Ronald J. A. (2010년 3월 2일). “A general introduction to the biochemistry of mitochondrial fatty acid β-oxidation”. 《Journal of Inherited Metabolic Disease》 (영어) 33 (5): 469–477. doi:10.1007/s10545-010-9061-2. ISSN 0141-8955. PMC 2950079. PMID 20195903.
- ↑ Fatland, B. L.; Ke J., Anderson MD., Mentzen WI., Cui LW., Allred CC., Johnston JL., Nikolau BJ., Wurtele ES. (2002). “Molecular Characterization of a Heteromeric ATP-Citrate Lyase That Generates Cytosolic Acetyl-Coenzyme a in Arabidopsis”. Plant Physiology (영어) 130 (2): 740. doi:10.1104/pp.008110. PMC 166603. PMID 12376641.
- ↑ 가 나 다 라 마 바 사 Stryer, Lubert (1995). 《Biochemistry.》 Four판. New York: W.H. Freeman and Company. 510–515, 559–565, 581–613, 614–623, 775–778쪽. ISBN 0-7167-2009-4.
- ↑ “Oxidation of fatty acids”.
- ↑ “Ketone body metabolism”. University of Waterloo. 2016년 9월 22일에 원본 문서에서 보존된 문서. 2018년 8월 1일에 확인함.
- ↑ 가 나 Ferre, P.; F. Foufelle (2007). “SREBP-1c Transcription Factor and Lipid Homeostasis: Clinical Perspective”. 《Hormone Research》 68 (2): 72–82. doi:10.1159/000100426. PMID 17344645. 2010년 8월 30일에 확인함.
this process is outlined graphically in page 73
- ↑ 가 나 Voet, Donald; Judith G. Voet; Charlotte W. Pratt (2006). 《Fundamentals of Biochemistry, 2nd Edition》. John Wiley and Sons, Inc. 547, 556쪽. ISBN 0-471-21495-7.
- ↑ Fatland, B. L. (2005). “Reverse Genetic Characterization of Cytosolic Acetyl-CoA Generation by ATP-Citrate Lyase in Arabidopsis”. 《The Plant Cell Online》 17: 182–203. doi:10.1105/tpc.104.026211. PMC 544498.
- ↑ Yi, C. H.; Vakifahmetoglu-Norberg, H.; Yuan, J. (2011년 1월 1일). “Integration of Apoptosis and Metabolism”. 《Cold Spring Harbor Symposia on Quantitative Biology》 (영어) 76: 375–387. doi:10.1101/sqb.2011.76.010777. ISSN 0091-7451. PMID 22089928. 2018년 6월 9일에 원본 문서에서 보존된 문서. 2018년 8월 1일에 확인함.
- ↑ Pettit, Flora H.; Pelley, John W.; Reed, Lester J. (1975년 7월 22일). “Regulation of pyruvate dehydrogenase kinase and phosphatase by acetyl-CoA/CoA and NADH/NAD ratios”. 《Biochemical and Biophysical Research Communications》 65 (2): 575–582. doi:10.1016/S0006-291X(75)80185-9.
- ↑ Jitrapakdee, Sarawut; Maurice, Martin St.; Rayment, Ivan; Cleland, W. Wallace; Wallace, John C.; Attwood, Paul V. (2008년 8월 1일). “Structure, Mechanism and Regulation of Pyruvate Carboxylase”. 《The Biochemical Journal》 413 (3): 369–387. doi:10.1042/BJ20080709. ISSN 0264-6021. PMC 2859305. PMID 18613815.
외부 링크
편집- 의학주제표목 (MeSH)의 Acetyl+Coenzyme+A