위장관 기질 종양
위장관 기질 종양(Gastrointestinal stromal tumor, GIST)은 위장관의 가장 흔한 중간엽 신생물이다. GIST는 Cajal의 평활근 박동조율기 간질 세포 또는 유사한 세포에서 발생한다. 이들은 KIT 유전자(85%), PDGFRA 유전자(10%), 또는 BRAF 키나제(희귀)의 돌연변이에 의해 행동이 유도되는 종양으로 정의된다. GIST의 95%가 KIT(CD117)에 대해 양성으로 염색 된다. 대부분(66%)은 위에서 발생하며 위 GIST는 위장관의 다른 곳에서 발견되는 종양보다 악성 가능성이 낮다.
 | |
|---|---|
| 다른 이름 | Gastrointestinal stromal tumor |
 | |
| 진료과 | 종양학 |
| 유사 질병 | 이소성 췌장[1] |
GIST는 1983년 진단 용어로 도입되었다. 1990년대 후반까지 위장관의 많은 비상피 종양은 "위장관 기질 종양"으로 불렸다. 조직병리학자는 현재 우리가 분자적으로 유사하지 않은 것으로 알려진 유형을 구체적으로 구별할 수 없었다. 그 후, CD34 및 이후 CD117은 다양한 유형을 구별할 수 있는 마커로 확인되었다. 또한 특정 치료법이 없는 경우 예후와 치료법에 제한적인 영향을 미쳤다.
GIST 생물학에 대한 이해는 GIST의 분자 기반이 확인되면서 크게 바뀌었다. 특히 c-KIT. 역사적으로, GIST의 분자적 정의 이전의 문헌 검토와 그 후 짧은 기간 동안 GIST의 70-80%가 양성이라고 주장했다. GIST에 대한 분자적 기반의 확인은 이전에 GIST로 간주되었던 많은 종양의 배제와 다른 유형의 육종 및 미분화 암종으로 분류되었던 훨씬 더 많은 수의 종양의 통합으로 이어졌다. 예를 들어, 위 및 소장 평활근육종 ( 평활근의 악성 종양)의 일부 이전 진단은 면역조직화학적 염색에 기초하여 GIST로 재분류된다. 모든 GIST 종양은 이제 악성 가능성이 있는 것으로 간주되며 GIST 종양은 "양성"으로 명확하게 분류될 수 없다. 따라서 모든 GIST는 AJCC(7판)/UICC의 암 병기 결정에 적합하다.[2] 그럼에도 불구하고, 다른 GIST는 기원 부위, 크기 및 유사분열 수치의 수에 따라 재발하거나 전이하는 경향에 대한 위험 평가가 다르다.
정의의 변경으로 인해 2000년 이전의 임상 치료 경로는 현재 시대에 대체로 정보가 없다.
징후 및 증상
편집GIST는 연하 장애, 위장관 출혈 또는 전이 (주로 간)를 나타낼 수 있다. 장 폐쇄는 종양의 외부 성장 패턴으로 인해 드물다. 종종 모호한 복통이나 불편감의 병력이 있으며 진단이 내려질 즈음에는 종양이 다소 커졌다.
병태생리학
편집GIST는 결합 조직의 종양, 즉 육종이다. 대부분의 위장관 종양과 달리 상피가 아니다. 약 70%는 위에서, 20%는 소장에서, 10% 미만은 식도에서 발생한다. 작은 종양은 일반적으로 양성이며 특히 세포 분열 속도가 느릴 때 더욱 그렇다. GIST 종양은 일반적으로 간 (사례의 28%) 및 대망, 소망 또는 장간막 (사례의 30%)으로 전이된다. 덜 흔한 전이 부위에는 폐, 피하 조직, 림프절 또는 뼈가 있다.[3]
GIST는 일반적으로 장의 자율 신경계의 일부인 Cajal(ICC)의 간질 세포에서 발생하는 것으로 생각된다. 그것들은 운동성 을 조절하는 심박조율기 기능을 한다.
약 85%의 GIST는 비정상적인 c-KIT 경로와 관련이 있다. c-KIT는 줄기 세포 인자 ( scf )라고 하는 성장 인자에 대한 막횡단 수용체를 인코딩하는 유전자이다. 비정상적인 c-KIT 경로는 가장 일반적으로(85%) 유전자 자체의 돌연변이에서 발생한다. c-KIT 관련 GIST의 더 작은 하위 집합은 면역 블로팅에 의해 발견되는 KIT 효소 경로의 구성적 활성과 관련이 있다. :1062c-KIT 제품/CD117은 ICC 및 다수의 다른 세포, 주로 골수 세포, 비만 세포, 멜라닌 세포 및 기타 여러 세포에서 발현된다. 그러나 장에서 CD117 에 양성인 대량 염색은 ICC 세포에서 발생하는 GIST일 가능성이 높다.
진단
편집CT 스캔은 종종 수행된다( 방사선과 섹션 참조).
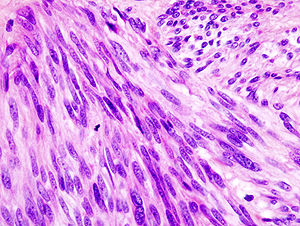
최종 진단은 내시경 적으로, CT 또는 초음파 유도를 통해 경피적으로 또는 수술 시에 얻을 수 있는 생검으로 이루어진다. 생검 샘플은 병리학자가 현미경으로 조사한다. 병리학자는 조직병리학을 검사하여 GIST(방추세포 70-80%, 상피양 20-30%)의 특성을 확인한다. 더 작은 종양은 일반적으로 장벽의 고유근층에 국한될 수 있다. 큰 것들은 장 벽에서 혈액 공급을 능가하는 지점까지 주로 바깥쪽으로 성장하고 내부에서 괴사(죽음)하여 결국 장 내강과 소통하게 될 수 있는 공동을 형성한다.
GIST가 의심되는 경우 — 유사한 종양 — 다른 원인과 달리) 병리학자는 면역조직화학 (분자 CD117 [ c-kit 이라고도 함]을 염색하는 특정 항체를 염색함 — 아래 참조)을 사용할 수 있다. 모든 GIST의 95%는 CD117-양성이다(다른 가능한 마커는 CD34, DOG-1, desmin 및 vimentin 포함). CD117 양성을 나타내는 다른 세포는 비만 세포이다.
방사선 영상의 목적은 병변을 찾고, 침범 징후를 평가하고, 전이를 감지하는 것이다. GIST의 특징은 종양의 크기와 기원에 따라 다르다. 직경은 수 밀리미터에서 30개 이상까지 다양하다. 센티미터. 더 큰 종양은 일반적으로 더 작고 더 나은 예후를 보이는 경향이 있는 우연히 발견된 종양과 대조적으로 증상을 유발한다. 큰 종양은 악성 행동을 보이는 경향이 있지만 작은 GIST는 임상적으로 공격적인 행동을 보일 수도 있다.
관리
편집국소적이고 절제 가능한 성인 GIST의 경우 해부학적으로나 생리학적으로 가능하다면 수술이 일차적 치료이다. :69수술은 잠재적으로 완치될 수 있지만 신중하게 선택된 상황에서 작은 종양의 경우 주의 깊게 기다리는 것이 고려될 수 있다. 수술 후 보조적 치료가 권장될 수 있다. 림프절 전이는 드물고 림프절의 일상적인 제거는 일반적으로 필요하지 않다. 망원경과 특수 기구를 사용한 최소 침습 복부 수술인 복강경 수술은 큰 절개 없이 이러한 종양을 제거하는 데 효과적인 것으로 나타났다. 종양 크기에 대한 정확한 수술 적응증의 임상 문제는 논란의 여지가 있다. 적절한 복강경 수술의 결정은 종양의 크기, 위치 및 성장 패턴에 영향을 받다.
방사선 요법은 역사적으로 IST에 대해 효과적이지 않았다 :1122GIST는 대부분의 화학요법 약물에 반응하지 않다. :11225% 미만의 응답으로. :1065그러나 GIST에서 임상적 이점이 있는 세 가지 약물( imatinib, sunitinib 및 regorafenib )이 확인되었다.
bcr-abl 억제를 기반으로 하는 만성 골수성 백혈병에 대해 초기에 판매된 경구 투여 약물인 Imatinib (Glivec/Gleevec)도 D842V 이외 의 c-kit 티로신 키나제 돌연변이와 PDGFRA 돌연변이를 모두 억제하며 여러 상황에서 GIST를 치료하는 데 유용하다. 이마티닙은 일부 선행 보조제 설정에서 사용되었다.[4] :23보조 치료 환경에서 대부분의 GIST 종양은 수술로 치유되며 보조 요법이 필요하지 않다.[5][6] 이에 대한 예외는 종양의 해부학적 위치로 인해 수술이 기술적으로 어렵거나 복잡하다는 것을 의미한다. 예를 들어, 직장 GIST는 종종 복부 회음부 절제 및 영구 장루를 포함하는 완전한 절제를 달성하기 위해 급진적 수술이 필요하다. 이러한 상황에서 신보조제 imatinib의 사용은 종양 크기와 유사분열 활성을 모두 상당히 감소시킬 수 있고 덜 근본적인 괄약근 보존 수술을 허용할 수 있다.[4]
상당한 비율의 GIST 종양은 다수의 검증된 위험 계층화 계획에 의해 추정된 바와 같이 높은 재발 위험을 가지며 보조 요법을 위해 고려될 수 있다.[6] 이러한 환경에서 이마티닙의 사용 가능성에 대한 결정을 뒷받침하는 선택 기준에는 종양 크기, 유사분열 속도 및 위치와 같은 병리학적 요인을 기반으로 한 위험 평가가 포함되어 GIST 환자의 재발 위험을 예측하는 데 사용할 수 있다. 종양 <2 5/50 HPF 미만의 유사분열율을 갖는 cm는 더 크거나 더 공격적인 종양보다 재발 위험이 더 낮은 것으로 나타났다. GIST의 외과적 절제 후 이마티닙을 사용한 보조 치료는 고위험군에서 질병 재발 위험을 감소시킨다. 일부 고위험 보조제 상황에서 이마티닙은 3년 동안 권장된다.
각주
편집- ↑ Yuan, Z; Chen, J; Zheng, Q; Huang, XY; Yang, Z; Tang, J (2009년 8월 7일). “Heterotopic pancreas in the gastrointestinal tract.”. 《World Journal of Gastroenterology》 15 (29): 3701–3. doi:10.3748/wjg.15.3701. PMC 2721251. PMID 19653355.
- ↑ AJCC manual
- ↑ Parab, Trisha M.; DeRogatis, Michael J.; Boaz, Alexander M.; Grasso, Salvatore A.; Issack, Paul S.; Duarte, David A.; Urayeneza, Olivier; Vahdat, Saloomeh; Qiao, Jian-Hua (February 2019). “Gastrointestinal stromal tumors: a comprehensive review”. 《Journal of Gastrointestinal Oncology》 10 (1): 144–154. doi:10.21037/jgo.2018.08.20. PMC 6351301. PMID 30788170.
- ↑ 가 나 “Surgical treatment of gastrointestinal stromal tumour of the rectum in the era of imatinib”. 《Br J Surg》 102 (8): 965–71. August 2015. doi:10.1002/bjs.9818. PMID 25970743.
- ↑ Joensuu, Heikki (2012년 6월 1일). “Adjuvant treatment of GIST: patient selection and treatment strategies”. 《Nature Reviews. Clinical Oncology》 9 (6): 351–358. doi:10.1038/nrclinonc.2012.74. ISSN 1759-4782. PMID 22525709.
- ↑ 가 나 Joensuu, Heikki (2012년 10월 22일). “Adjuvant therapy for high-risk gastrointestinal stromal tumour: considerations for optimal management”. 《Drugs》 72 (15): 1953–1963. doi:10.2165/11635590-000000000-00000. ISSN 0012-6667. PMID 22994537.
일반 출처
편집- “Gastrointestinal stromal tumors (GIST): C-kit mutations, CD117 expression, differential diagnosis and targeted cancer therapy with Imatinib” (PDF). 《Pathol Oncol Res》 9 (1): 13–9. 2003. doi:10.1007/BF03033708. PMID 12704441.
- “Gastrointestinal stromal tumors (GIST): a model for molecule-based diagnosis and treatment of solid tumors”. 《Cancer Sci.》 94 (4): 315–20. Apr 2003. doi:10.1111/j.1349-7006.2003.tb01439.x. PMID 12824897.