핵염기
핵염기(核鹽基, 영어: nucleobase)는 뉴클레오사이드의 구성 성분으로 질소를 함유하고 있는 생물학적 화합물이다. 뉴클레오사이드는 뉴클레오타이드의 구성 성분이며, 뉴클레오타이드는 핵산을 구성하는 단위체로 작용한다. 핵염기는 질소 염기(窒素鹽基, 영어: nitrogenous base) 또는 간단히 염기(鹽基, 영어: base)로도 알려져 있다. 핵염기가 염기쌍을 형성하고, 서로 겹쳐 쌓이게 하는 능력은 리보핵산(RNA) 및 디옥시리보핵산(DNA)와 같은 긴 사슬 구조를 형성하게 한다.


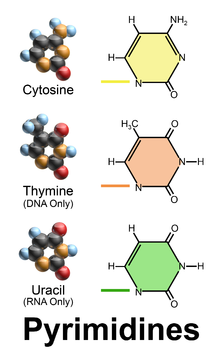
아데닌(A), 구아닌(G), 사이토신(C), 티민(T), 유라실(U)의 5가지 핵염기를 주요 염기라고 한다. 이들 주요 염기들은 유전 암호의 기본 단위로 기능하며, 아데닌(A), 구아닌(G), 사이토신(C), 티민(T)은 DNA에서 발견되고, 아데닌(A), 구아닌(G), 사이토신(C), 유라실(U)은 RNA에서 발견된다. 티민과 유라실은 티민이 고리의 5번 위치에 메틸기를 가지고 있다는 점을 제외하면 동일하다.
아데닌과 구아닌은 퓨린에서 유래한 융합된 고리 골격 구조를 가지고 있기 때문에 퓨린 염기라고 한다. 마찬가지로 사이토신, 유라실, 티민은 피리미딘에서 유래한 단일 고리 골격 구조를 가지고 있기 때문에 피리미딘 염기라고 한다. 퓨린 계열의 염기는 아데닌의 6번 탄소와 구아닌의 2번 탄소에 아미노기를 특징적으로 가지고 있다.[1] 전형적인 이중나선 DNA에서 아데닌(A)은 티민(T)과 염기쌍을 형성하고, 구아닌(G)은 사이토신(C)과 염기쌍을 형성한다. 이러한 퓨린 염기와 피리미딘 염기는 상보적인 염기쌍을 형성하여 DNA 이중나선의 두 가닥을 수소 결합으로 연결한다. DNA에서 퓨린 계열 염기와 피리미딘 계열 염기 사이에 상보적인 염기쌍이 형성되므로 DNA 이중나선의 지름은 2 nm로 일정하다. 상보적인 염기의 아미노기와 카보닐기 사이에 수소 결합을 형성하게 되는데, 아데닌(A)과 티민(T) 사이에는 2개의 수소 결합을, 구아닌(G)과 사이토신(C) 사이에는 3개의 수소 결합을 형성한다.
아데닌, 구아닌, 잔틴, 하이포잔틴, 퓨린, 2,6-다이아미노퓨린, 6,8-다이아미노퓨린과 같은 핵염기들은 지구에서 뿐만 아니라 우주에서 형성되었을 수도 있다.[2][3][4]
핵염기에서 염기라는 용어는 산-염기 반응에서 이들 화합물의 화학적 특성을 반영하지만, 이러한 특성은 핵염기의 생물학적 기능의 대부분을 이해하는 데 그렇게 중요하지는 않다.
구조
편집핵산 구조의 측면에서 인산 분자는 2개의 인접한 뉴클레오타이드 단량체의 5탄당 부분을 연속적으로 연결하여 긴 사슬의 생체분자를 생성한다. 5탄당(리보스 또는 디옥시리보스)과 인산으로 구성된 사슬은 단일 가닥 또는 이중나선 생체분자를 위한 골격을 생성한다. DNA 이중나선에서 2개의 가닥은 양 말단의 방향이 서로 반대인 역평행 구조이며, 이는 2개의 염기 사이에 상보적인 염기쌍을 형성할 수 있도록 하고, DNA의 유전 정보의 복제 또는 전사에 필수적이다.
변형된 핵염기
편집DNA와 RNA는 핵산 사슬이 형성된 후에 변형된(주요 염기가 아닌) 염기를 함유하고 있다. DNA에서 가장 일반적인 변형된 염기는 5-메틸사이토신(m5C)이다. RNA에는 뉴클레오사이드인 슈도유리딘(Ψ), 다이하이드로유리딘(D), 이노신(I), 7-메틸구아노신(m7G)에 포함된 것들을 포함하여 많은 변형된 염기들이 있다.[5][6]
하이포잔틴 및 잔틴은 돌연변이원을 통해 생성되는 많은 염기들 중 두 가지이며, 둘 다 탈아미노화(아미노기를 카보닐기로 치환)을 통해 생성된다. 하이포잔틴은 아데닌으로부터 생성되고, 잔틴은 구아닌으로부터 생성되며,[7] 유라실은 사이토신의 탈아미노화에 의해 생성된다.
변형된 퓨린 핵염기
편집이들은 변형된 아데노신, 구아노신의 예이다.
| 핵염기 | 하이포잔틴 |
잔틴 |
7-메틸구아닌 |
| 뉴클레오사이드 | 이노신 I |
잔토신 X |
7-메틸구아노신 m7G |
변형된 피리미딘 핵염기
편집이들은 변형된 사이토신, 티민, 유리딘의 예이다.
| 핵염기 | 5,6-다이하이드로유라실 |
5-메틸사이토신 |
5-하이드록시메틸사이토신 |
| 뉴클레오사이드 | 다이하이드로유리딘 D |
5-메틸사이티딘 m5C |
인공 핵염기
편집수많은 핵염기 유사체들이 존재한다. 가장 일반적인 응용 분야는 마이크로어레이에서 cRNA 또는 cDNA를 표시하는 데 사용되는 아미노알릴 뉴클레오타이드와 같이 직접 또는 간접적으로 형광 프로브로 사용된다. 몇몇 그룹은 유전 암호를 확장하기 위해 대안적인 추가 염기쌍, 예를 들어 아이소구아닌 및 아이소사이토신 또는 형광성 2-아미노-6-(2-싸이엔일)퓨린 및 피롤-2-카브알데하이드를 연구하고 있다.
의학에서는 여러 가지 뉴클레오타이드 유사체가 항암제 및 항바이러스제로 사용된다. 바이러스의 중합효소는 이들 화합물을 비주요 염기와 통합시킨다. 이들 화합물은 뉴클레오타이드로 전환됨으로써 세포에서 활성화된다. 하전된 뉴클레오타이드는 세포막을 쉽게 통과할 수 없기 때문에 이들 화합물은 뉴클레오사이드로 투여된다. 2014년 5월을 기준으로 적어도 하나의 새로운 염기쌍이 발표되었다.[8]
핵염기와 리보스의 생물 발생 이전의 축합
편집생명이 어떻게 생겨났는지를 이해하려면 그럴듯한 생물 발생 이전 조건에서 생명의 핵심 구성 요소들을 형성할 수 있는 화학적 경로에 대한 지식이 필요하다. RNA 세계 가설에 따르면 자유 부동(浮動) 리보뉴클레오타이드는 원시 수프에 존재했었다. 이들은 직렬로 결합해서 RNA를 형성하는 기본 분자였다. RNA처럼 복잡한 분자는 반응성이 물리화학적 과정에 의해 지배되는 작은 분자로부터 생성되었음이 틀림없다. RNA는 퓨린 뉴클레오타이드와 피리미딘 뉴클레오타이드로 구성되며, 둘 다 신뢰할 수 있는 정보 전달, 따라서 다윈의 자연선택과 진화에 필요하다. 남(Nam) 등[9]은 RNA 형성으로 이어지는 핵심 단계인 미세 물방울에서 핵염기와 리보스의 직접적인 축합에 의해 리보뉴클레오사이드가 생성되는 것을 입증했다. 벡커(Becker) 등은 습식-건식 사이클을 사용하여 유사한 결과를 얻어냈다.[10]
같이 보기
편집각주
편집- ↑ Berg JM, Tymoczko JL, Stryer L. “Section 25.2, Purine Bases Can Be Synthesized de Novo or Recycled by Salvage Pathways.”. 《Biochemistry. 5th Edition》. 2019년 12월 11일에 확인함.
- ↑ Callahan MP, Smith KE, Cleaves HJ, Ruzicka J, Stern JC, Glavin DP, House CH, Dworkin JP (August 2011). “Carbonaceous meteorites contain a wide range of extraterrestrial nucleobases”. 《Proceedings of the National Academy of Sciences of the United States of America》 (PNAS) 108 (34): 13995–8. doi:10.1073/pnas.1106493108. PMC 3161613. PMID 21836052. 2011년 9월 18일에 원본 문서에서 보존된 문서. 2011년 8월 15일에 확인함.
- ↑ Steigerwald, John (2011년 8월 8일). “NASA Researchers: DNA Building Blocks Can Be Made in Space”. NASA. 2015년 6월 23일에 원본 문서에서 보존된 문서. 2011년 8월 10일에 확인함.
- ↑ ScienceDaily Staff (2011년 8월 9일). “DNA Building Blocks Can Be Made in Space, NASA Evidence Suggests”. 《ScienceDaily》. 2011년 8월 9일에 확인함.
- ↑ Stavely, Brian E. “BIOL2060: Translation”. 《www.mun.ca》. 2020년 8월 5일에 원본 문서에서 보존된 문서. 2020년 8월 17일에 확인함.
- ↑ "Role of 5' mRNA and 5' U snRNA cap structures in regulation of gene expression" – Research – Retrieved 13 December 2010.
- ↑ Nguyen T, Brunson D, Crespi CL, Penman BW, Wishnok JS, Tannenbaum SR (April 1992). “DNA damage and mutation in human cells exposed to nitric oxide in vitro”. 《Proceedings of the National Academy of Sciences of the United States of America》 89 (7): 3030–4. doi:10.1073/pnas.89.7.3030. PMC 48797. PMID 1557408.
- ↑ Malyshev DA, Dhami K, Lavergne T, Chen T, Dai N, Foster JM, Corrêa IR & Romesberg FE (May 2014). “A semi-synthetic organism with an expanded genetic alphabet”. 《Nature》 509 (7500): 385–8. doi:10.1038/nature13314. PMC 4058825. PMID 24805238.
- ↑ Nam I, Nam HG, Zare RN. Abiotic synthesis of purine and pyrimidine ribonucleosides in aqueous microdroplets. Proc Natl Acad Sci U S A. 2018 Jan 2;115(1):36-40. doi: 10.1073/pnas.1718559115. Epub 2017 Dec 18. PMID: 29255025; PMCID: PMC5776833
- ↑ Becker S, Feldmann J, Wiedemann S, Okamura H, Schneider C, Iwan K, Crisp A, Rossa M, Amatov T, Carell T. Unified prebiotically plausible synthesis of pyrimidine and purine RNA ribonucleotides. Science. 2019 Oct 4;366(6461):76-82. doi: 10.1126/science.aax2747. PMID: 31604305.
외부 링크
편집위키미디어 공용에 핵염기 관련 미디어 분류가 있습니다.