산화·환원 반응
산화·환원 반응(酸化還元反應, 영어: Redox, reduction-oxidation)은 원자의 산화수가 달라지는 화학 반응이다. 산화·환원 반응은 화학종 사이의 실제 또는 형식적인 전자 이동을 특징으로 하며, 가장 흔히 한 종(환원제)은 산화(전자 손실)를 겪고 다른 종(산화제)은 환원(전자획득)을 겪는다.[1] 전자가 제거된 화학종은 산화된 화학종이라고 하고 전자가 추가된 화학종은 환원된 화학종이라고 한다. 다시 말해서:
- 산화(Oxidation)는 분자, 원자 또는 이온이 산소를 얻거나 수소 또는 전자를 '잃는' 것을 말한다.
- 환원(Reduction)은 분자, 원자 또는 이온이 산소를 잃거나 수소 또는 전자를 '얻는' 것을 말한다.
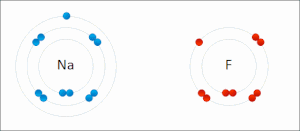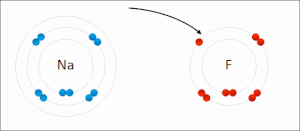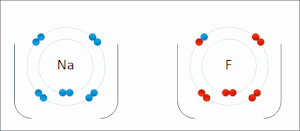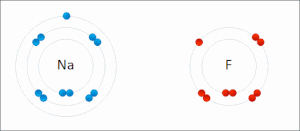
많은 유기 화학에서의 반응은 산화 상태의 변화로 인한 산화 환원 반응이지만 뚜렷한 전자 이동이 없다. 예를 들어, 산소 분자로 나무를 연소시키는 동안 나무에 있는 탄소 원자의 산화 상태는 증가하고 산소 원자의 산화 상태는 이산화탄소와 물이 형성됨에 따라 감소한다. 산소 원자는 환원되어 전자를 얻고 탄소 원자는 산화되어 전자를 잃는다. 따라서 이 반응에서 산소는 산화제이고 탄소는 환원제이다.[2]
산화 반응은 일반적으로 산소 분자로부터 산화물의 형성과 관련이 있지만 다른 화학종이 동일한 기능을 할 수 있기 때문에 이러한 반응에 산소가 반드시 포함되는 것은 아니다.
산화·환원 반응은 녹 형성에서와 같이 상대적으로 느리게 또는 연료 연소의 경우에서와 같이 훨씬 더 빠르게 발생할 수 있다. 탄소를 산화시켜 이산화탄소(CO2)를 생성하거나 탄소를 수소에 의해 환원시켜 메탄(CH4)을 생성하는 것과 같은 간단한 산화·환원 과정과 인체에서 포도당(C6H12O6)의 산화와 같은 복잡한 과정이 있다. 물의 결합 에너지와 이온화 에너지 분석을 통해 산화·환원 전위를 계산할 수 있다.[3][4]
정의
편집원래 고전적인 의미의 산화와 환원은 산소 원자의 이동을 말하였지만, 이후에는 산소의 이동보다는 수소와 전자, 특히 전자의 이동에 주목한다. 산화, 환원 반응이 일어날 때는 그 물질의 산화수가 변하며, 산화수의 변화를 기준으로 산화, 환원이 일어났음을 예측하기도 함.
산화제와 환원제
편집산화 환원 과정에서 환원제는 전자를 산화제로 전달한다. 따라서 반응에서 환원제는 전자를 잃고 산화되고, 산화제는 전자를 얻고 환원된다. 특정 반응에 관여하는 한 쌍의 산화제와 환원제를 산화 환원 쌍이라고 한다.[5]
산화제
편집다른 물질을 산화시킬 수 있는 물질을 산화제라 한다. 산화제는 다른 물질로부터 전자를 빼앗아 산화시키고 자신은 환원되는 물질이다. 산화제는 전자를 "수용"하기 때문에 전자수용체라고도 한다. 산소는 대표적인 산화제이다.
환원제
편집다른 물질을 환원시킬 수 있는 물질을 환원제라 한다. 환원제는 전자를 다른 물질로 이동시켜 환원시키고 자신은 산화되는 물질이다. 환원제는 전자를 주기 때문에 전자공여체라고도 한다.
연소
편집산화는 반응 속도에 따라서 빠른 산화와 느린 산화로 구분될 수 있다. 특히 빠른 산화이면 연소라고 한다.
연소의 예시로 일산화 탄소의 생성이 있다. 탄소 원자는 결정 구조 속에 들어있다. 이때 산소 분자 하나가 탄소 원자에 접근하면 개개의 산소 원자들은 자신의 파트너를 떠나서 탄소 원자 하나와 새롭게 결합한다. 이렇게 탄생한 탄소-산소 원자쌍이 바로 일산화탄소 기체 분자이며, 화학식으로는 CO로 표기한다.
이때 산소 원자끼리, 혹은 탄소 원자끼리 당기는 힘보다는 탄소 원자와 산소 원자 사이의 인력이 훨씬 강하다. 그래서 산소 원자가 탄소 원자 근처로 접근한 때에는 에너지를 조금밖에 가지고 있지 않지만, 산소와 탄소가 결합할 때에는 큰 에너지가 필요하여 주변의 원자들에게 여파를 미치게 되는데 이것은 운동에너지를 가지게 된다는 것이다. 이 과정에서 (거의 대부분의 경우에) 열에너지가 방출되는데 특정한 조건에서는 에너지가 매우 많이 방출되면서 불꽃의 형태로 빛을 방출하기도 한다. 이 모든 과정을 요약한 것이 연소이다.
일상생활 속의 산화·환원
편집각주
편집- ↑ “Redox Reactions”. wiley.com. 2012년 5월 30일에 원본 문서에서 보존된 문서. 2012년 5월 9일에 확인함.
- ↑ Haustein, Catherine Hinga (2014). 〈Oxidation-reduction reaction〉. K. Lee Lerner; Brenda Wilmoth Lerner. 《The Gale Encyclopedia of Science》 5판. Farmington Hills, MI: Gale Group.
- ↑ Schmidt-Rohr, K. (2018). “How Batteries Store and Release Energy: Explaining Basic Electrochemistry”. 《J. Chem. Educ.》 95 (10): 1801–1810. Bibcode:2018JChEd..95.1801S. doi:10.1021/acs.jchemed.8b00479.
- ↑ Schmidt-Rohr, K. (2015). “Why Combustions Are Always Exothermic, Yielding About 418 kJ per Mole of O2”. 《J. Chem. Educ.》 92 (12): 2094–2099. Bibcode:2015JChEd..92.2094S. doi:10.1021/acs.jchemed.5b00333.
- ↑ Pingarrón, José M.; Labuda, Ján; Barek, Jiří; Brett, Christopher M. A.; Camões, Maria Filomena; Fojta, Miroslav; Hibbert, D. Brynn (2020). “Terminology of electrochemical methods of analysis (IUPAC Recommendations 2019)”. 《Pure and Applied Chemistry》 92 (4): 641–694. doi:10.1515/pac-2018-0109.
같이 보기
편집외부 링크
편집- 위키미디어 공용에 산화·환원 반응 관련 미디어 분류가 있습니다.