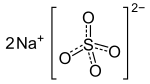
황산 나트륨
화합물
이 문서는 영어 위키백과의 sodium sulfate 문서를 번역하여 문서의 내용을 확장할 필요가 있습니다. |
황산 나트륨(sodium sulfate)은 Na2SO4 화학식을 지니는 나트륨의 황산염이다. 유리, 군청 따위의 제조에 쓰이며 빛깔이 없는 단사 정계의 결정이다.
| |||
| 이름 | |||
|---|---|---|---|
| 별칭
Sodium sulphate
Sulfate of sodium Thenardite (mineral) Glauber's salt (decahydrate) Sal mirabilis (decahydrate) Mirabilite (decahydrate mineral) Disodium sulfate | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.928 | ||
| E 번호 | E514(i) (산도 조절제, ...) | ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| Na2SO4 | |||
| 몰 질량 | 142.04 g/mol (anhydrous) 322.20 g/mol (decahydrate) | ||
| 겉보기 | white crystalline solid hygroscopic | ||
| 냄새 | odorless | ||
| 밀도 | 2.664 g/cm3 (anhydrous) 1.464 g/cm3 (decahydrate) | ||
| 녹는점 | 884 °C (1,623 °F; 1,157 K) (anhydrous) 32.38 °C (decahydrate) | ||
| 끓는점 | 1,429 °C (2,604 °F; 1,702 K) (anhydrous) | ||
| anhydrous: 4.76 g/100 mL (0 °C) 28.1 g/100 mL (25 °C)[1] 42.7 g/100 mL (100 °C) heptahydrate: 19.5 g/100 mL (0 °C) 44 g/100 mL (20 °C) | |||
| 용해도 | insoluble in 에탄올 soluble in glycerol, water and hydrogen iodide | ||
자화율 (χ)
|
−52.0·10−6 cm3/mol | ||
굴절률 (nD)
|
1.468 (anhydrous) 1.394 (decahydrate) | ||
| 구조 | |||
| orthorhombic (anhydrous)[2] monoclinic (decahydrate) | |||
| 약리학 | |||
| A06AD13 (WHO) A12CA02 | |||
| 위험 | |||
| 주요 위험 | Irritant | ||
| 물질 안전 보건 자료 | ICSC 0952 | ||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | Non-flammable | ||
| 관련 화합물 | |||
다른 음이온
|
Sodium selenate Sodium tellurate | ||
다른 양이온
|
Lithium sulfate Potassium sulfate Rubidium sulfate Caesium sulfate | ||
관련 화합물
|
Sodium bisulfate Sodium sulfite Sodium persulfate | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
안전
편집황산 나트륨이 일반적으로 무독성으로 알려져 있으나[3] 주의해서 다룰 필요가 있다. 소량일지라도 일시적인 천식이나 눈의 염증을 일으킬 수 있다. 이러한 위험은 눈 보호대나 종이형 마스크를 이용하여 예방할 수 있다. 운송에는 제한이 없으며 유럽 연합 위험 규정이나 유럽 연합 안전 규정에 적용되지 않는다.[4]
각주
편집- ↑ cite National Center for Biotechnology Information. PubChem Compound Summary for CID 24436, Sodium sulfate. https://pubchem.ncbi.nlm.nih.gov/compound/Sodium-sulfate. Accessed Nov. 2, 2020.
- ↑ Zachariasen, W. H.; Ziegler, G. E. (1932). “The crystal structure of anhydrous sodium sulfate Na2SO4”. 《Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie》 (Wiesbaden: Akademische Verlagsgesellschaft) 81: 92–101. doi:10.1524/zkri.1932.81.1.92. S2CID 102107891.
- ↑ “Sodium sulfate (WHO Food Additives Series 44)”. 세계 보건 기구. 2000. 2007년 6월 6일에 확인함.
- ↑ “MSDS Sodium Sulfate Anhydrous”. James T Baker. 2006. 2003년 6월 19일에 원본 문서에서 보존된 문서. 2007년 4월 21일에 확인함.
외부 링크
편집- (영어) Sodium sulfate information of Airborne Industrial Minerals
- (영어) Sodium sulfate website of Elementis Chromium
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |